Spektra
Introduction
Dnes se astrofyzika ani moderní vědecké laboratoře neobejdou bez kvalitního spektrometru, který vědcům umožní provádět spektrální (případně též frekvenční) analýzu. Ze spektra potom vyčteme informace o míře zastoupení jednotlivých frekvencí, z čehož můžeme vyvozovat další informace, jako např. chemické složení vesmírných objektů, pohyb zdroje atd. – pochopitelně v závislosti na daném oboru (astrofyzika, biofyzika; rovněž v akustice se provádí frekvenční analýza…).
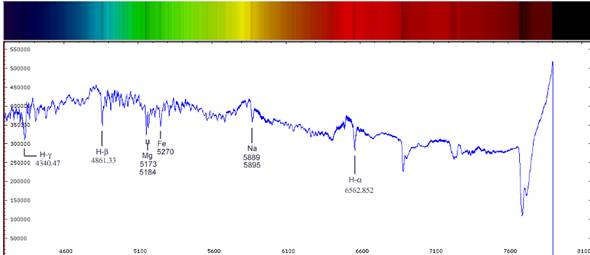
Pro spektrální analýzu světla jsou klíčové obsažené spektrální čáry, jejichž původ zůstával dlouho záhadou. Pomohla je objasnit až kvantová hypotéza ve spojení se zákonem zachování energie.
Podle kvantové hypotézy se světlo nevyzařuje spojitě, ale po jakýchsi „balíčcích energie“, kterým říkáme fotony. Energie Ef každého fotonu souvisí pouze s jeho frekvencí f podle vztahu
Ef = hf
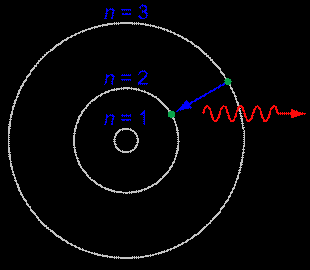
kde h = 6,63·10−34 J·s je Planckova konstanta. Dokonce podle kvantové fyziky ani elektrony v atomových obalech nemůžou nabývat libovolné energie a mohou se nacházet výhradně v určitých energetických stavech, resp. hladinách (závislých na druhu atomu), případně mezi nimi skokově přecházet. Při přeskocích vždy musí zůstat zachován v platnosti zákon zachování energie, který vyžaduje buď vznik a vyzáření (tj. emisi) fotonu o příslušné energii, a tedy frekvenci, nebo pohlcení takového fotonu (tzv. absorpci). Označíme-li energie dvou různých dovolených energetických hladin E1 a E2 (E2>E1), pak lze zákon zachování energie vyjádřit rovnicí
|
Ef = ΔE = E3 − E2 = hf |
Kdy dojde k emisi a kdy k absorpci, určují tzv. Kirchhofovy zákony spektrální analýzy.
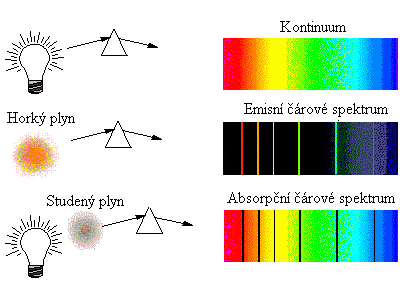
- Rozžhavené těleso (např. hvězda, vlákno žárovky) o určité teplotě T vyzařuje všechny frekvence, které ve spektru pozorujeme jako tzv. kontinuum.
- Horký plyn (ve vesmíru např. oblak horkého vodíku) vyzařuje pouze některé barvy (tedy určité dovolené frekvence), které ve spektru spatříme jako jasné emisní čáry na temném pozadí.
- Studený plyn (ve vesmíru např. oblak vodíku o teplotě T1 mezi Zemí a vzdálenou hvězdou o teplotě T>T1) pohltí vybrané barvy z kontinua (odpovídající frekvence), tedy ve spektru najdeme tzv. tmavé absorpční čáry.
Pro nejjednodušší systém a zároveň nejrozšířenější prvek ve vesmíru vodík (tedy systém proton–elektron) lze pozorované frekvence spektrálních čar přesně vystihnout jediným vzorcem. Ve vzdálené laboratorní úloze si můžete frekvence zastoupených čar z pořízeného spektra odečíst a na jejich základě příslušný vztah objevit (heuristický přístup), anebo prostudovat odvození vztahu a experimentálně jeho platnost ověřit (verifikační přístup). Vyberte si.
Heuristický přístup – doporučujeme pro vážnější zájemce o; fyziku
Pokračujte návštěvou vzdálené laboratoře na UK MFF, seznamte se s návodem a proveďte zadané úkoly v části pro SŠ.
Verifikační přístup – potvrzení platnosti Ritzova-Rydbergova kombinačního principu a Rydbergovy formule
Pokračujte prostudováním fyzikálního základu.
Seznamte se s návodem a proveďte vzdálené měření, resp. zadané úkoly.
| Tyto stránky a vzdálené experimenty vznikly v rámci projektu č. 957/2012 Výuka kvantové fyziky metodou integrovaného e-learningu, financovaného Fondem rozvoje vysokých škol (www.frvs.cz). |
